Introducción
El tejido óseo es un sitio frecuente de extensión metastásica, especialmente a la columna vertebral. Se ha estimado que en autopsias cerca del 35% de los pacientes con cáncer de próstata tienen metástasis al momento de la muerte1, y en los casos de tumores resistentes al tratamiento hormonal el porcentaje de enfermedad metastásica asciende al 80%2. El mecanismo más frecuente de diseminación de células cancerígenas es por vía hematógena, por los vasos segmentarios o de forma retrógrada desde los vasos pélvicos por el plexo venoso avalvular de Batson. Esto explica que la ubicación más común de estas lesiones metastásicas por cáncer de próstata sea la región lumbosacra, a diferencia de las metástasis por otros tipos de tumores, que muestran una mayor predilección por la columna torácica3. La estructura vertebral más afectada es el cuerpo vertebral, hasta 20 veces más común que la afectación de los elementos posteriores de la vértebra4.
Los pacientes con cáncer de próstata se presentan en distintos escenarios clínicos. Inicialmente la enfermedad es localizada, asintomática y sensible al manejo hormonal. Posteriormente se extiende localmente o a distancia. Además, sin importar si se ha hecho metastásico o no, el cáncer de próstata se vuelve resistente a las hormonas5.
Es importante resaltar que desde el momento en que la enfermedad genera metástasis, la supervivencia aproximada es de 3-5 años. Así mismo, en los primeros dos años el 41,9% de los pacientes presentará eventos óseos, que pueden llevar a fracturas patológicas o compresión medular, y requerir cirugía para estabilización o reconstrucción ósea, descompresión o radioterapia5. Así mismo, una de cada tres metástasis óseas serán sintomáticas y resultarán en compresión medular o inestabilidad mecánica de la columna vertebral6.
La compresión de la médula espinal es una complicación neurológica común de patologías neoplásicas avanzadas. Se presenta en el 5-10% de los pacientes con cualquier malignidad. En los hombres, la principal causa es el cáncer de pulmón, seguida por el cáncer de próstata, que corresponde al 1-12% de los casos. Además, en el 12-19% de los pacientes con cáncer de próstata la compresión medular es el modo de presentación de la enfermedad7.
La compresión medular metastásica es una emergencia oncológica, y el pronóstico de recuperación funcional está en relación con la rapidez en la que se pueda iniciar el manejo especializado. Por esto es fundamental la sensibilización del paciente y el personal de salud en identificar oportunamente las manifestaciones clínicas y evitar retrasos en la atención y el tratamiento8.
Todas las intervenciones que se realicen en el paciente con enfermedad metastásica son de carácter paliativo y tienen como objetivo mejorar la calidad de vida en el paciente con enfermedad tumoral avanzada, controlando el dolor, evitando las complicaciones como la parálisis motora y permitiendo conservar la funcionalidad e independencia4. El objetivo del presente trabajo fue describir las herramientas fundamentales para el tratamiento integral de pacientes con cáncer de próstata y compresión medular.
Método
Realizamos esta revisión de alcance de acuerdo con las recomendaciones del Instituto Joanna Briggs.
Criterios de elegibilidad
- Participantes. Estudios con evidencia de herramientas usadas para el manejo integral de pacientes con compresión medular secundaria a cáncer de próstata metastásico.
- Concepto. Nos enfocamos en evaluar la información presente que evalúa las herramientas usadas para el manejo de pacientes con compresión medular secundario por cáncer de próstata.
- Contexto. Incluimos todos los idiomas.
Fuentes de información
Incluimos cualquier estudio que fuera específico a nuestros objetivos. Se realizó una búsqueda bibliográfica exhaustiva siguiendo los encabezamientos de temas médicos (MeSH), el idioma Emtree y las palabras de texto relacionadas. Buscamos en Medline (Ovid), Embase, Lilacs y el Registro Cochrane Central de Ensayos Controlados (Central) desde el inicio hasta la actualidad. Se usó la combinación de palabras claves: metástasis, cáncer de próstata, compresión medular y manejo quirúrgico.
Recolección de datos
Dos investigadores revisaron cada referencia por título y resumen. Luego escanearon los textos completos de los estudios relevantes y aplicaron criterios de inclusión y exclusión preespecificados. Los desacuerdos se resolvieron por consenso. Dos revisores capacitados que utilizaron un formulario estandarizado extrajeron de forma independiente la información basada en el título, los objetivos, los criterios de inclusión y exclusión, las definiciones de resultados, los resultados, la fuente de financiamiento y otros hallazgos clave.
Síntesis de resultados
Mostramos los resultados de forma descriptiva. Los resultados se clasificaron en categorías conceptuales principales para facilitar la comprensión.
Manifestaciones clínicas
Los pacientes con metástasis a columna pueden ser asintomáticos, y estas lesiones pueden ser descubiertas como un hallazgo incidental en el 36% de los casos4, así como en el 20% de los pacientes se puede encontrar un déficit neurológico agudo como primera manifestación clínica de un cáncer, hasta ese momento desconocido8.
El síntoma más frecuente es el dolor axial, el cual puede estar presente en el 95% de los pacientes. Generalmente tiene un inicio insidioso, lentamente progresivo, y se puede presentar incluso hasta dos meses previos a desarrollar cualquier otro síntoma. El dolor es el síntoma inicial más frecuente en el paciente con lesiones metastásicas, se debe tener un alto índice de sospecha en todo aquel paciente con dolor espinal en presencia de signos de alarma relacionados con patología tumoral como la edad mayor de 50 años, pérdida de peso, dolor nocturno o en reposo y antecedente personal de cáncer9.
Otra manifestación clínica relacionada con la presencia de metástasis espinales es el déficit asociado con la compresión de las estructuras neurales. El grado de disfunción neurológica está en relación con la gravedad de la compresión neural. Este puede comprender desde dolor de características neuropáticas hasta la parálisis completa de las extremidades, junto con la pérdida de la función sensitiva y esfinteriana. Además, se puede manifestar con dificultad para caminar, ponerse de pie o presentar mayor dificultad para realizar transiciones, incontinencia o retención urinaria. La disfunción neurológica esta en relación con el grado de la compresión neural10.
Evaluación
Ante la sospecha de una lesión metastásica asociada con síntomas neurológicos debe solicitarse en las primeras 24 horas una resonancia magnética (RM) de columna total, ya que puede presentarse compresión neural en niveles no consecutivos hasta en el 20-35% de los pacientes1. La RM presenta una sensibilidad del 93% y especificidad del 97% para el diagnóstico de lesiones tumorales en columna. La tomografía computarizada de columna vertebral como estudio complementario es de utilidad para establecer el grado de destrucción ósea y determinar inestabilidad mecánica de acuerdo con la naturaleza de las lesiones: si estas son formadoras de hueso (blásticas), forma más común asociada con el cáncer de próstata, líticas (destructoras de hueso) o mixtas.
Pronóstico
La compresión medular causa daño neurológico que puede llegar a ser irreversible, disminuye la calidad de vida y además disminuye la supervivencia de los pacientes2. Esta patología se considera una emergencia oncológica, y por ende requiere un tratamiento inmediato y agresivo. Se debe incluir en el equipo de manejo al médico general, oncólogo, radio-oncólogo, cirujano de columna, médico especialista en dolor y urólogo. Los pilares del tratamiento son los esteroides, la cirugía y la radioterapia, y la terapia de privación androgénica3,4.
Los tres objetivos principales del tratamiento serán preservar o recuperar la función neurológica, aliviar el dolor y mejorar la calidad de vida del paciente. Hasta el 70-75% de los pacientes mejorarán si la lesión medular no se ha establecido. Sin embargo, a pesar de los avances en el diagnóstico y el tratamiento de la entidad, poco ha cambiado la posibilidad de recuperación neurológica en pacientes con lesión medular establecida7,3.
El pronóstico neurológico y la supervivencia de estos pacientes dependerá de la gravedad del déficit motor encontrado al momento del diagnóstico, la presencia de disfunción autonómica, la sensibilidad a la terapia hormonal y la respuesta inicial al manejo proporcionado. Si el paciente puede caminar al momento del diagnóstico, hasta el 70-92% lo será después del tratamiento. Si se presenta déficit motor incompleto, el 44-83% conservarán la capacidad de marcha, y si se presenta con plejía, solo el 20-22% caminará posteriormente5–7. Por otra parte, si los pacientes se presentan con disfunción autonómica, como la retención urinaria, hasta el 66% no caminará tras el tratamiento. Además, si el paciente se presenta sin déficit neurológico, la supervivencia media será de 18,9 meses, mientras que si se presenta con este, será de 3,9 meses. Otro factor que determina el pronóstico es la respuesta completa al tratamiento: si hay respuesta, la supervivencia media será de 9,5 meses, mientras que si no responde será de dos meses. Así mismo, los pacientes que han recibido deprivación androgénica previa tienen una supervivencia media de 16 a 42 meses vs. 6 a 7,6 meses en quienes no recibieron esta terapia hormonal7.
En diferentes estudios, los pacientes con compresión medular por cáncer de próstata que recibieron dexametasona, descompresión medular con o sin estabilización y rehabilitación presentaron una mejor respuesta neurológica y una mayor supervivencia global, claramente dependiendo del estado tumoral y el tiempo de intervención7,2.
Recomendaciones de manejo
Cáncer de próstata metastásico a hueso sensible a hormonas
Para los pacientes con cáncer de próstata metastásico a hueso, con enfermedad sensible a las hormonas, sintomáticos, el tratamiento inmediato es obligatorio. Se recomienda el tratamiento sistémico inmediato con terapia de deprivación androgénica para paliar síntomas y reducir el riesgo de secuelas serias potenciales por enfermedad avanzada, como compresión medular, fracturas patológicas u obstrucción ureteral. Así mismo, se reconoce que no hay evidencia de alta calidad a favor de alguna terapia, excepto para los pacientes con compresión medular, para quienes la orquiectomía bilateral o los antagonistas de hormona luteinizante son las opciones preferidas. Se debe ofrecer dichos antagonistas, especialmente para los pacientes con compresión espinal inminente u obstrucción del tracto de salida de la vejiga. En este grupo de pacientes se debe ofrecer cirugía y radioterapia local a cualquier paciente con enfermedad metastásica con evidencia de complicaciones inminentes como la compresión medular o las fracturas patológicas. Respecto al ácido zoledrónico en pacientes con enfermedad sensible hormonas, se aclara que este no aumenta el tiempo al primer evento óseo, ni mejora la supervivencia global, al compararlo con placebo. Esto se basa en los resultados de los estudios CALGB 90202 Alliance y STAMPEDE. No hay información disponible acerca del uso del denosumab en este grupo de pacientes8–20.
Cáncer de próstata metastásico a hueso resistente a la castración
En el escenario de enfermedad metastásica resistente a la castración, se recomienda ofrecer agentes protectores óseos a pacientes con enfermedad resistente a la castración y metástasis esqueléticas para prevenir complicaciones óseas. El ácido zoledrónico en dosis de 4 mg cada 4 semanas por 15 meses ha demostrado superioridad vs. el placebo para: reducir la incidencia de eventos óseos, 38 vs. 49% (p = 0,029); reducir la incidencia de fracturas patológicas, 13,1 vs. 22,1% (p = 0,015); aumentar el tiempo al primer evento óseo, 488 vs. 321 días (p = 0,009), y disminuir el dolor asociado a las metástasis óseas. Sin embargo se ha demostrado que no tiene ningún efecto en la progresión de la enfermedad, ni en la supervivencia de estos pacientes21. Por su parte, el denosumab en dosis de 120 mg cada 4 semanas ha demostrado ser superior al ácido zoledrónico para retrasar o prevenir tanto el primero como los eventos óseos subsecuentes y disminuir los marcadores de resorción ósea en el mismo escenario. Sin embargo, tampoco ha demostrado tener un efecto en la supervivencia22–24. Cuando se prescriben estos agentes protectores óseos, se recomienda monitorizar los niveles séricos de calcio y ofrecer suplementos con calcio y vitamina D.
Tratamiento integral
Las guías de la Asociación Europea de Urología sobre el cáncer de próstata, en su versión 2021, mencionan que, para pacientes con metástasis óseas, las complicaciones más comunes son el colapso vertebral, la deformidad vertebral, las fracturas patológicas y la compresión medular. Para aquellos pacientes con fracturas espinales patológicas dolorosas, se propone cirugía medular, esteroides a dosis elevadas y radioterapia después de la cirugía, para mejorar el compromiso neurológico, el dolor y la calidad de vida8.
De tal manera que el tratamiento de la compresión medular maligna debe incluir: a) el manejo del dolor oncológico; b) las medidas terapéuticas para la prevención del colapso vertebral y el establecimiento o progresión del déficit neurológico; c) la prolongación de la supervivencia, y d) la paliación de los síntomas residuales. En un paciente con alta sospecha clínica de compresión medular metastásica se inicia el uso de esteroides con el objetivo de reducir el edema medular y preservar la función neurológica. Se recomienda el uso de dosis intermedias para evitar los efectos secundarios propios del uso de esteroides a dosis altas, dado que se obtienen los mismos beneficios, por eso la indicación es iniciar dexametasona a dosis inicial 16 mg intravenosa seguido de 8 mg cada 12 h (Fig. 1)25.
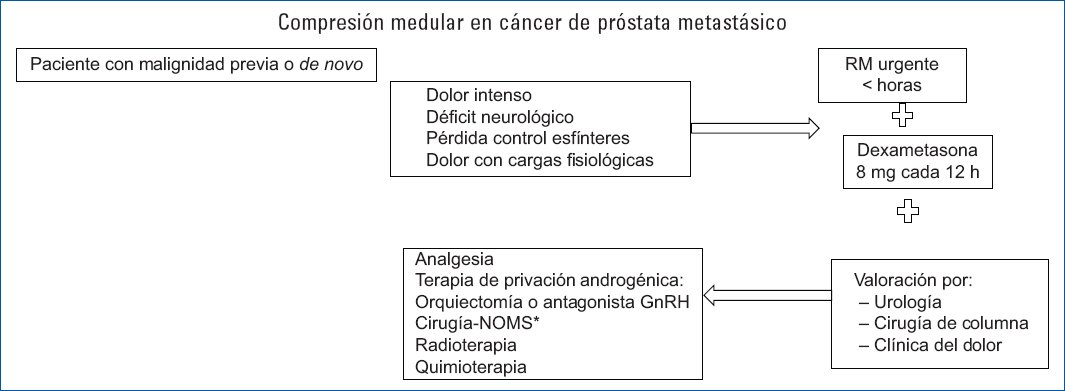
Figura 1. Flujograma de manejo.
*Neurologic status Oncology, Mechanic, Systemic.
GnRH: hormona liberadora de gonadotropina; RM: resonancia magnética.
Laufer et al.26 proponen un enfoque del paciente con metástasis en columna bajo el esquema NOMS (acrónimo de Neurologic status, Oncology, Mechanic y Systemic), en el cual se inpidualiza cada caso clínico al tener en cuenta el estado dinámico de la enfermedad para determinar el tratamiento de las metástasis de la columna que integre estos cuatro puntos de decisión; además, proporciona una herramienta para una comunicación efectiva interdisciplinaria que permita desarrollar planes de tratamiento inpidualizados.
El estado neurológico se determina por los hallazgos al examen físico y la imagen de RM, estableciendo como compresión de alto grado las lesiones tumorales que ocupan el canal raquídeo y desplazan la médula espinal. En estas lesiones, si el paciente es candidato para manejo quirúrgico, debe ser llevado a cirugía para descompresión neural urgente. Si por el contrario, por el tiempo de evolución, el déficit neurológico no es recuperable y ya hay una mielopatía establecida o las condiciones clínicas no permiten que el paciente sea llevado a cirugía de forma segura, se indica citorreducción con radioterapia, terapia hormonal si previamente no la ha recibido y tratamiento con esteroides4.
El estado oncológico hace referencia a la naturaleza histológica del tumor, la agresividad y la respuesta a las terapias no quirúrgicas. El cáncer de próstata tiene una sensibilidad intermedia a la radioterapia convencional de rayo externo, por lo que se debe considerar como parte del esquema de tratamiento, ya sea como terapia única o como adyuvante al manejo quirúrgico27. Como se mencionó anteriormente, la sensibilidad a la terapia hormonal se considera un factor pronóstico, teniendo los tumores resistentes a hormonas una supervivencia menor, mayores tasas de complicaciones, en especial de metástasis y mielopatía, y menor respuesta al tratamiento28.
La inestabilidad mecánica se define como «pérdida de la integridad espinal como resultado de un proceso neoplásico que se asocia con dolor relacionado con el movimiento, deformidad sintomática o progresiva o compromiso bajo cargas fisiológicas». Se determina objetivamente con la escala SINS (Spinal Instability Neoplasic Score)29 (Tabla 1). Un puntaje mayor a 7 sugiere inestabilidad espinal y requiere estabilización quirúrgica. El cáncer de próstata genera frecuentemente metástasis blásticas que causan menos inestabilidad mecánica.
Tabla 1. Escala SINS (Spinal Instability Neoplastic Score)
| Característica | Puntaje |
|---|---|
| Ubicación | |
| Sitio de transición (Occipucio-C2, C7-T2, T11-L1, L5-S1) | 3 |
| Móvil (C3-C6, L2-L4) | 2 |
| Semirrígido (T3-T10) | 1 |
| Rígido (S2-S5) | 2 |
| Dolor con movimiento o carga | |
| Sí (dolor mecánico) | 3 |
| No (dolor ocasional, no mecánico) | 1 |
| Sin dolor | 0 |
| Lesión ósea | |
| Lítica | 2 |
| Mixta (lítica/blástica) | 1 |
| Blástica | 0 |
| Alineación radiográfica espinal | |
| Subluxación/traslación | 4 |
| Deformidad de novo (cifosis/escoliosis) | 2 |
| Alineación normal | 0 |
| Colapso cuerpo vertebral | |
| > 50% | 3 |
| < 50% | 2 |
| Sin colapso con > 50% compromiso cuerpo vertebral | 1 |
| Ninguno | 0 |
| Compromiso elementos espinales posteriores | |
| Bilaterales | 3 |
| Unilaterales | 1 |
| Ninguno | 0 |
| Puntaje total | Estabilidad |
| 0-6 | Estable |
| 7-12 | Indeterminado |
| 13-18 | Inestable |
El estado sistémico se establece teniendo en cuenta el compromiso de la enfermedad sistémica, el grado de diseminación del tumor, las comorbilidades médicas y la capacidad del paciente de tolerar una intervención quirúrgica.
Manejo quirúrgico
Tradicionalmente las indicaciones de manejo quirúrgico en enfermedad metastásica en columna vertebral son: a) déficit agudo asociado a compresión neurológica; b) inestabilidad mecánica, y c) dolor incontrolable4,30. Sin embargo, para decidir si es o no candidato para ser llevado a cirugía se debe considerar que el paciente tenga factores pronósticos de supervivencia favorables, con expectativa mayor a 3-6 meses, la posibilidad de recuperación neurológica de acuerdo con el grado de funcionalidad y tiempo de evolución del déficit, y la capacidad del paciente de tolerar la cirugía de acuerdo con sus comorbilidades y reserva fisiológica28.
Decidir si un paciente requiere y se beneficia de la intervención quirúrgica se logra al correlacionar las manifestaciones clínicas y las imágenes diagnósticas con el uso de escalas de puntuación, las cuales pueden objetivar el estado clínico el pronóstico, y establecer las estrategias de manejo. Son múltiples las escalas usadas en patología oncológica para establecer pronóstico de supervivencia, con resultados dispares entre ellas, sin embargo la escala de Tokuhashi revisada31 es de fácil aplicación y ha sido validada para establecer pronóstico en enfermedad metastásica espinal (Tabla 2). La puntuación resultante proporciona una supervivencia estimada. Pacientes con una supervivencia mayor a seis meses se consideran candidatos a manejo quirúrgico, mientras que aquellos con un pronóstico menor de seis meses tienen indicación de manejo médico paliativo.
Tabla 2. Escala de Tokuhashi revisada
| Característica | Puntaje |
|---|---|
| Condición general (Karnoffsky) | |
| Pobre (10-40%) | 0 |
| Moderado (50-70%) | 1 |
| Bueno (80-100%) | 2 |
| Numero de focos metástasis extraespinales | |
| ≥ 3 | 0 |
| 1-2 | 1 |
| 0 | 2 |
| Número de metástasis en cuerpos vertebrales | |
| ≥ 3 | 0 |
| 1-2 | 1 |
| 0 | 2 |
| Metástasis a otros órganos internos | |
| No resecable | 0 |
| Resecable | 1 |
| Ausente | 2 |
| Sitio primario de malignidad | |
| Pulmón, osteosarcoma, estomago, | 0 |
| vejiga, esófago, páncreas | |
| Hígado, vesícula biliar, no identificado | 1 |
| Otros | 3 |
| Útero, riñón | 4 |
| Tiroides, mama, próstata, carcinoide | 5 |
| Parálisis | |
| Completa (Frankel A, B) | 0 |
| Incompleta (Frankel C, D) | 1 |
| Sin parálisis (Frankel E) | 2 |
| Puntaje total | Sobrevida (meses) |
| 0-8 | < 6 |
| 9-11 | 6-12 |
| 2-15 | > 12 |
La cirugía para manejo de metástasis espinales en pacientes seleccionados muestra beneficios importantes en mejorar la calidad de vida, mejorar o preservar la función motora, la marcha y la función vesical, con una relativa baja mortalidad y morbilidad28. La mortalidad asociada a la cirugía está por debajo del 7% y las complicaciones generales alrededor del 32%, con un porcentaje de complicaciones mayores del 18%32. Se deben considerar las opciones de manejo de cirugía mínimamente invasiva, la cirugía de separación (resección del tejido tumoral que se encuentra alrededor de la médula a través de un abordaje posterior) y la descompresión por vía posterior en contraste con las descompresiones circunferenciales (anterior y posterior), ya que pueden dar resultados similares con menos morbilidad y convalecencia, incluso en pacientes con menor supervivencia.
Cuando existe un déficit neurológico asociado con compresión maligna en pacientes que tienen expectativa de recuperación neurológica, los procedimientos quirúrgicos para descompresión directa, asociados o no con estabilización cirugía, han mostrado superioridad frente a la radioterapia sola en la recuperación funcional. En un ensayo clínico aleatorizado Patchell et al.33 demostraron que los pacientes llevados a cirugía presentaban capacidad de conservar la marcha (84 vs. 57%; p = 0,001) o recuperarla si ya tenían déficit (62 vs. 19%; p = 0,01), con un efecto más sostenido en el tiempo (122 vs. 13 días; p = 0,03) en comparación con los pacientes que solo recibieron radioterapia. Clarke et al. encontraron que los pacientes sometidos a cirugía tenían una mejoría funcional (el 57% recuperaban la marcha) o la conservaban, el 48% mejoraban un grado o más de la escala de Frankel y solo un 3% empeoraban. Así mismo el 45% recuperaban la continencia, y como efecto adicional de la cirugía había un mejor control del dolor con menor consumo de opioides28.
En el manejo quirúrgico de las lesiones metastásicas en columna por cáncer de próstata se deben tener algunas consideraciones especiales dadas las características propias de este tipo de lesión. Además, la toma de decisiones quirúrgicas va a depender de la inpidualización de la enfermedad paciente y su contexto. Las lesiones blásticas son la forma más frecuente de presentación, siendo intrínsecamente más estables. Es probable que si se realiza una descompresión limitada y no desestabilizadora, en muchos casos no sea necesaria la instrumentación o la aumentación vertebral, como tampoco una corpectomía, obteniendo buenos resultados con procedimientos que tienen menores tasas de complicaciones28. Las descompresiones circunferenciales, a través uno o dos abordajes, tienen mayor morbilidad, sangrado y tiempos quirúrgicos más prolongados. La laminectomía sola para descompresión directa o indirecta y la cirugía de separación neural son opciones viables cuando la estabilidad mecánica no está comprometida. Además, el cáncer de próstata tiene predilección por la columna lumbar, comprometiendo las raíces espinales y la cauda equina más que la médula, por lo que la descompresión anterior (corpectomía) es menos relevante que la descompresión posterior (laminectomía).
Cuando el problema depende de la estabilidad de los segmentos vertebrales está indicada la instrumentación espinal, sea por técnicas convencionales abiertas o mínimamente invasivas percutáneas, y en pacientes con supervivencia estimada menor a un año no es necesaria la aplicación de injertos óseos ni artrodesis. A pesar de que la mayoría de las lesiones son blásticas, en estadios avanzados y especialmente en tumores resistentes a hormonas se pueden presentar lesiones líticas. Estas pueden ser manejadas con técnicas percutáneas de aumentación vertebral con cemento óseo como la vertebroplastia o la cifoplastia, llevando a disminución del dolor y estabilidad mecánica con tasas mínimas de complicaciones.
Conclusiones
La compresión de la médula espinal es una complicación neurológica común de patologías neoplásicas avanzadas, y se puede presentar en pacientes con cáncer de próstata previamente conocido, o constituir la forma de presentación de este. La compresión medular causa daño neurológico que puede llegar a ser irreversible, disminuye la calidad de vida y además reduce la supervivencia de los pacientes. El pronóstico neurológico y la supervivencia dependen del tiempo de compresión, el déficit inicial y el estadio hormonal del paciente. El manejo de esta entidad debe ser multidisciplinario e inmediato, y se basa en esteroides, radioterapia con o sin cirugía, y terapia de privación androgénica. Por último, se deben tomar medidas para la prevención y el diagnóstico temprano de la compresión medular en pacientes en riesgo, o con síntomas previos, considerando el escenario clínico de la enfermedad.
Financiamiento
Los autores declaran no haber recibido financiamiento para este estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
