Introducción
El cáncer de próstata (CaP) es el segundo cáncer más comúnmente diagnosticado en hombres, seguido del cáncer de pulmón. Para el año 2022, GLOBOCAN informó que la incidencia de CaP fue del 14,2%, la mortalidad de 4,1% y la prevalencia de 126,7 × 100.000 hab, posicionándose como la cuarta causa de muerte por cáncer entre los hombres en todo el mundo1.
Existen factores de riesgo asociados al desarrollo de CaP: entre ellos destaca la edad mayor a 65 años, un historial familiar de cáncer incrementa el riesgo 2,5 veces, se ha evidenciado que el origen étnico también influye (los hombres del sur y este de Asia tienen tasas más bajas de mortalidad2, mientas que los hombres de raza negra tienen un riesgo mayor de progresión a la enfermedad metastásica3), un patrón dietético basado en un alto consumo de carne procesada y lácteos con alto contenido en ácidos grasos saturados y bajo consumo de verduras y frutas favorece mecanismos que estimulan la proliferación de células cancerosas y los procesos de angiogénesis4; adicionalmente el consumo de alcohol y de tabaco se asocian en el desarrollo de CaP.
La detección y estadificación clínica del CaP se basa en los niveles séricos del antígeno prostático específico (PSA), la puntuación de Gleason tras la biopsia y la estadificación TNM5; sin embargo, estos métodos no siempre son exactos, lo que lleva a diagnósticos y tratamientos subóptimos.
La creciente introducción a la tecnología molecular ha permitido la identificación de un amplio espectro de alteraciones genómicas, incluidas mutaciones, variaciones del número de copias (CNV), translocaciones y fusiones en múltiples genes, revolucionado el campo de la medicina de precisión6, al permitir estudios que identifiquen las modificaciones que suceden en el ADN, el ARN, las proteínas y otras moléculas biológicas, desempeñando un papel fundamental para la detección, cribado y clasificación de pacientes, así como en la evaluación de la respuesta al tratamiento de manera eficiente, en menor tiempo y con mayor precisión7.
En este artículo abordaremos la información disponible sobre los OMIC disponibles para el diagnóstico del CaP y las alteraciones genéticas que se presentan con mayor frecuencia.
Genética del cáncer de próstata
El desarrollo del CaP desde un punto de vista molecular es heterogéneo; esto en la medida que existen una diversidad de alteraciones moleculares inter- e intratumorales, y al proceso genómico dinámico y evolutivo que enfrenta8, la patogénesis y el desarrollo, las células cancerígenas se desarrollan a partir de mutaciones, que son alteraciones en la secuencia y/o estructura de los genes9. Se clasifican en mutaciones germinales y mutaciones somáticas: las germinales que se producen durante el intercambio genético entre el óvulo y el espermatozoide y tienen un 50% de probabilidad de ser trasmitidas a la siguiente generación, mientras que las mutaciones somáticas se originan en un tejido en desarrollo, generan células idénticas, que tienen esta mutación pero no están presentes en todas las células del individuo y por lo tanto no se heredan, y pueden ser ocasionadas por factores ambientales o disrupciones durante el proceso de replicación del ADN10.
Es importante entender que la teoría para el desarrollo en la mayoría de los tumores sólidos se fundamenta en que su origen es una sola célula, la cual adquiere potencial de crecimiento mediante la acumulación de mutaciones genéticas y alteraciones epigenéticas hereditarias que modifican el sistema celular11.
Aproximadamente el 50% de todos de los cánceres de próstata tanto primarios como avanzados presentan reordenamiento TMPRSS2:ERG, que es el lugar de la actividad promotora del crecimiento del oncogén ERG bajo el control de los elementos reguladores de TMPRSS2 sensible a los andrógenos. Los CaP primarios con reordenamiento ERG presentan frecuentemente deleciones en los cromosomas 6q, 8p, 10q y 13q que incluyen genes como NKX3-1, PTEN, BRCA2 y RB112. El otro 50% sin reordenamiento ERG se subclasifica según la sobreexpresión de SPINK110, mutaciones SPOP y aberraciones del número de copias somáticas seleccionadas, que a menudo son mutuamente excluyentes (Fig. 1A).
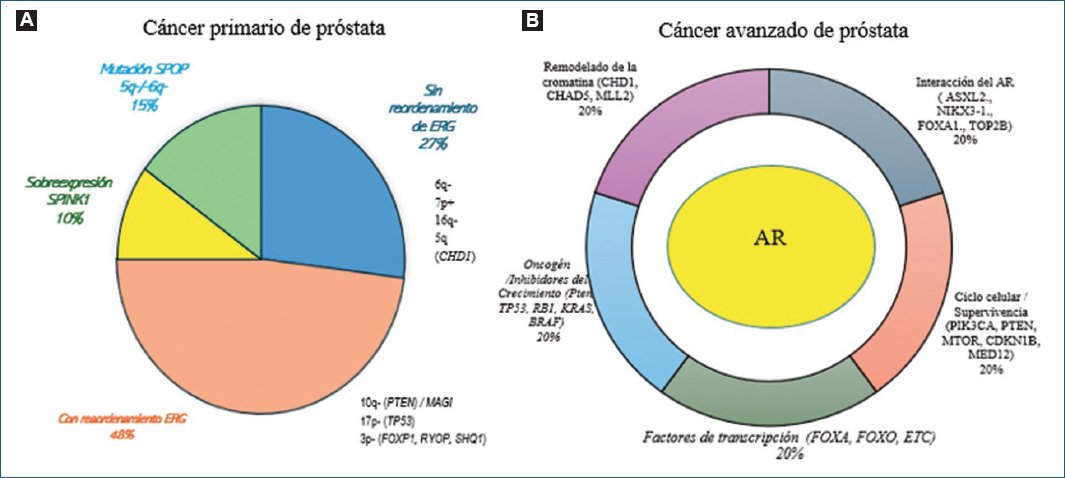
Figura 1. Distribución de las alteraciones genéticas en el cáncer de próstata inicial y avanzado. A: porcentajes de alteraciones genéticas existentes en cáncer primario de próstata con relación con el reordenamiento del gen ERG. B: porcentaje de alteraciones genéticas en cáncer de próstata avanzado relacionados con la expresión del oncogén AR, relacionado con las funciones celulares.
La supervivencia, el crecimiento y la actividad proliferativa de las células de CaP dependen en gran medida de los andrógenos que activan el receptor de andrógenos (AR) en las células tumorales, que provocan la proliferación celular y progresión tumoral13. La figura 1B representa los cambios que se ha identificado en el CaP avanzado y que contribuyen al alto grado de inestabilidad genética, debido al aumento de la accesibilidad del ADN a factores que inducen roturas del ADN, encontrándose alteraciones principalmente en la vía de señalización de los andrógenos, las vías de señalización de la fosfatidilinositol 3-cinasa (PI3K) y AKT, en los factores de transcripción y modificadores de la cromatina y heterogeneidad clonal de los oncogenes y genes supresores de tumores y en el ciclo celular14.
La regulación genética mediada por epigenética tiene un papel trascendental durante los procesos de desarrollo embrionario que frecuentemente se reactiva y opera durante el inicio y la progresión del cáncer. Los reguladores epigenéticos que incluyen la metilación del ADN, las modificaciones de histonas, los ARN no codificantes y los remodeladores de la cromatina, los cuales están regulados de manera diferencial en los tejidos cancerosos en comparación con sus contrapartes normales, lo que contribuye al inicio y la progresión del cáncer15.
La secuenciación de nueva generación, una herramienta para el diagnóstico
El diagnóstico, estadificación y tratamiento del CaP se realiza considerando los niveles séricos del PSA, la puntuación de Gleason tras la biopsia y pruebas de imágenes complementarias5; sin embargo, estas herramientas no son exactas, por lo que los avances de la tecnología han permitido una evolución significativa enfocada en el diagnóstico molecular de precisión impulsada por la llegada de la tecnología ómica, que ha revolucionado el estudio el cáncer.
La evolución de las técnicas para el diagnóstico molecular (Fig. 2) incluyen la inmunohistoquímica (IHQ), la hibridación in situ (FISH, CISH, DISH), la reacción en cadena de la polimerasa (PCR), la secuenciación de Sanger y la secuenciación de próxima generación, conocida como NGS (next generation sequencing)16, esta última ha permitido secuenciar gran cantidad de segmentos de ADN de forma masiva y en paralelo, en menor cantidad de tiempo y a un menor costo por base17, de manera que para el CaP esta tecnología ha permitido la identificación de fusiones génicas, amplificaciones, deleciones hemi- y homocigotas y/o variantes puntuales en un solo procedimiento18.
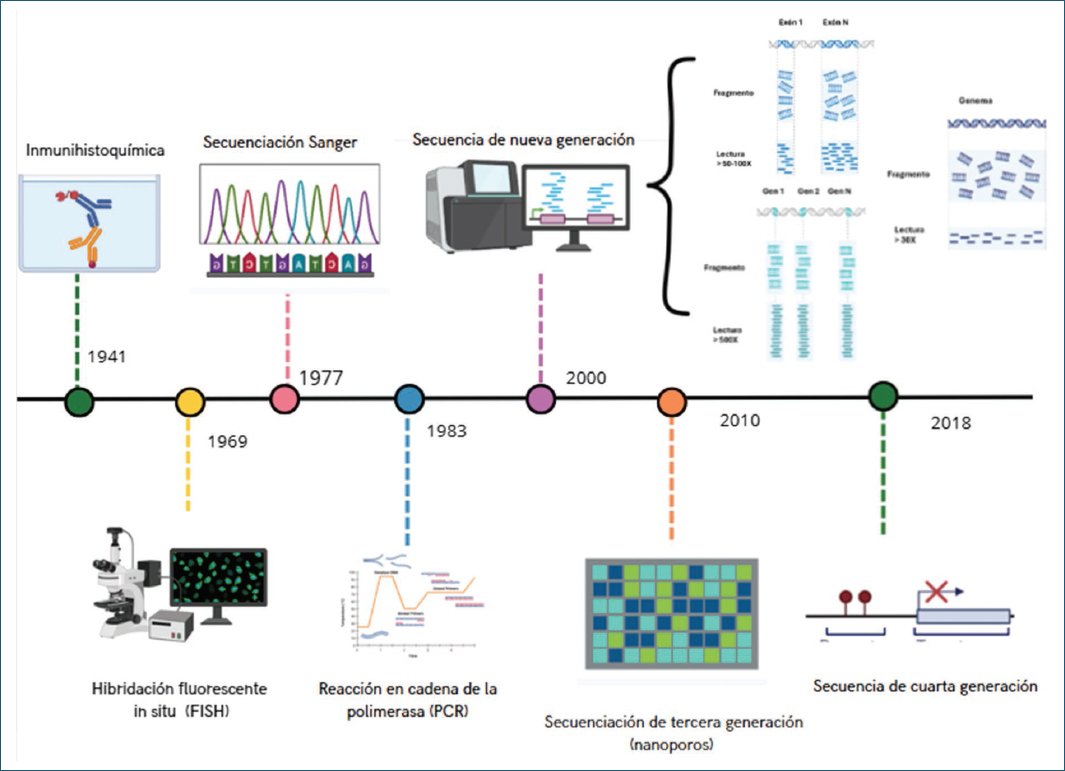
Figura 2. Evolución de las técnicas de diagnóstico molecular. Esta línea del tiempo describe las técnicas usadas en el diagnóstico de cáncer de próstata, desde la inmunohistoquímica hasta la era de las OMIC.
Inmersos en la práctica clínica se han implementado principalmente cuatro tipos de NGS, los cuales se oferta por las distintas casas comerciales en virtud de la cantidad de datos, la duración de las lecturas, el tiempo para el desarrollo y la técnica implementada:
- – Secuenciación de paneles de genes. Contienen cebadores o sondas para un grupo conocido de genes, esto permiten secuenciar mutaciones conocidas (hot spots), genes completos, detectar CNV y translocaciones. La ventaja de este método es que permite una secuenciación con gran cobertura y profundidad de lectura, permitiendo la detección de variantes de muy baja frecuenciaz17.
- – Secuenciación del exoma (WES). Permite la amplificación de exones mediante PCR o su captura mediante sondas, permite identificar de genes en enfermedades mendelianas altamente penetrantes, ya que se concentra en solo el 1% del genoma y está restringido a variantes codificantes y de sitios de empalme en genes anotados. Esto es de gran utilidad en pacientes que padecen enfermedades de gran heterogeneidad genética. Su principal desventaja es el costo elevado19.
- – Secuenciación completa del genoma (WGS). Tiene la ventaja de una cobertura continua y la identificación de variantes a lo largo de todo el genoma, permitiendo detectar variantes no exónicas, mejorar la detección de las CNV y un mayor rendimiento sobre la WES. Sin embargo, la mayor limitación está determinada por la longitud de lectura de la secuencia, que al ser de alrededor de 200 pb puede llevar a que la alineación ocurra en una región del genoma que no corresponda20.
- – Secuenciación del transcriptoma (WTS). Permite capturar ARN codificante y no codificante y cuantificar la heterogeneidad de la expresión genética en células, tejidos y órganos y permite la detección de nuevas estructuras de genes, isoformas alternativas de splicing, fusiones génicas, polimorfismos de varios nucleótidos, indeles y expresión específica de alelos21.
La enorme cantidad de datos generados, principalmente por las NGS, exige nuevos desarrollos de software y hardware, con el desarrollo y uso de herramientas matemáticas, inmersas en la estadística y bioinformática que involucran inteligencia artificial, aprendizaje automático y hardware de red neuronal dedicado, para analizar mejor los grandes datos22.
Paneles genéticos para el diagnóstico
La identificación de biomarcadores celulares, bioquímicos y moleculares se consideran instrumento de fácil aplicabilidad para el diagnóstico, monitoreo y tratamiento del cáncer22. Dentro de sus ventajas en el CaP se encuentran el bajo costo, la metodología no invasiva y el análisis de múltiples alteraciones en poco tiempo, que prevenir biopsias de próstata innecesarias, y que genera informaciones relevantes en el pronóstico de la sobrevivencia y el monitoreo del tratamiento23.
Los genes, dependiendo del tipo de variante adquirida, podrían estar relacionados con la afección desde su origen somática o germinal; existe recomendaciones sobre el uso de los paneles que contiene genes de la línea germinal para el CaP en hombres con CaP avanzado, para guiar las decisiones de tratamiento y manejo de la enfermedad, mientras que en hombres sin CaP con antecedentes familiares de cáncer permite establecer medidas de prevención para la detección precoz y la vigilancia activa una vez diagnosticado24, mientras que el CaP metastásico resistente a la castración (mCRPC) presenta aberraciones en los genes de reparación del ADN (BRCA2, BRCA1, ATM, CHEK2 y HOXB13) con una frecuencia del 20 al 30%25.
En el año 2018, el Consenso sobre el Cáncer de Próstata de Filadelfia recomendó realizar paneles amplios (germinales y somáticos) en pacientes con CaP metastásico, utilizando la NGS para identificar mutaciones que puedan ser confirmadas como mutaciones germinales en pacientes con antecedentes familiares (padre o hermano menor de 60 años) y para pacientes con CaP no metastásico el uso de paneles genéticos se realizaría considerando situaciones específicas como ascendencia judía ashkenazí, enfermedad avanzada (T3a o superior), patología intraductal/ductal, y un Gleason igual o superior a 826. Para el año 2020, la Sociedad Europea de Oncología Médica (ESMO) propone tres niveles de recomendaciones para el uso de NGS en los distintos tipos de cáncer, específicamente para el CaP: recomienda realizar NGS para evaluar el estado mutacional de, al menos, BRCA1/2, además de considerar el uso de paneles más grandes que engloben el gen PTEN, genes de reparación del ADN y la firma MSI en caso de CaP avanzado, evaluando el costo-efectividad de la intervención27.
Considerando el rol en el diagnóstico del CaP, se realizó una búsqueda sobre los paneles genéticos disponibles por las distintas casas comerciales (Tabla 1), clasificándolos con base en la muestra biológica (saliva o sangre, tejidos y orina), el tiempo que se requiere para el procesamiento de la muestra y la utilidad clínica. Se identificó que los paneles genéticos que utilizan muestra de sangre y/o saliva analizan genes de la línea germinal, lo que orienta el diagnóstico de tumores con riesgo hereditario. Los paneles genéticos que emplean muestras de tejidos consideran mutaciones genéticas somáticas y/o germinales, lo que permite la estadificación de la afección y un enfoque terapéutico. Los paneles genéticos con biomarcadores en orina permiten establecer la probabilidad de desarrollar la enfermedad, ya que permiten la identificación de mutaciones somáticas, con la finalidad de evitar exámenes invasivos, por ello se recomiendan tanto para guiar decisiones de tratamiento en cáncer metastásico como para evaluar el riesgo hereditario en hombres con antecedentes familiares o factores de riesgo específicos.
Tabla 1. Paneles genéticos disponibles para el diagnóstico de CaP
| Tipo de muestra | Plataforma | Tiempo | Objetivo de la prueba | Instrumentos | Genes | Link cobertura | |
|---|---|---|---|---|---|---|---|
| Biomarcadores en orina | ExoDx Prostate IntelliScore | 5 días | Establece la distinción entre la enfermedad prostática benigna y la enfermedad maligna de bajo grado | Exosome Diagnostics, Inc. | PCA3, ERG, SPDEF | https://www.exosomedx.com/ | |
| My Prostate Score 2.0 | 5 a 7 días | Permite la predicción clara y altamente individualizada del riesgo de un paciente de tener CaP clínicamente significativo | LynxDx | T2:ERG, SCHLAP1, OR51E2, APOC1, PCAT14, CAMKK2, PCA3, NKAIN1, B3GNT6, TFF3, SPON2, PCGEM1, TRGV9, TMSB15A, ERG, KLK3, KLK4, HOXC6 | https://www.lynxdx.com/about-us/ | ||
| Progensa PCA3 | 5 días | Establecer la probabilidad de desarrollar CaP | Hologic | PCA3, PSA | https://www.hologic.com/ | ||
| SelectMDx | 7 días | Probabilidad de detectar CaP tras una biopsia, determinando la probabilidad de enfermedad de alto grado | MDxHealth | HOXC6, DLX1 | https://ferrerone.com/producto/selectmdx/ | ||
| TMPRSS2: ERG | 7 días | Establecer la probabilidad de desarrollar CaP | Oncore pro | TMPRSS2, ERG | https://biocare.net/oncore- pro/ | ||
| Biomarcadores en sangre y/o saliva | CellSearch Circulation Tumor Cells | 1 sem | Predictor sólido e independiente de la supervivencia general y libre de progresión en el cáncer de mama, próstata y colorrectal metastásico | Menarini Silicon Biosystems, Inc. | Células tumorales circulantes | https://www.cellsearchctc.com/clinical- applications/clinical- applications- overview | |
| Hereditary Cancer Panel | 2 sem | Asociación con el riesgo de tipos comunes de cáncer hereditario: cáncer de mama, cáncer de ovario, cáncer de útero, cáncer colorrectal, melanoma, cáncer de páncreas, cáncer de estómago y cáncer de próstata | Color | APC, ATM, BAP1, BARD1, BMPR1A, BRCA1, BRCA2, BRIP1, CDH1, CDK4, CDKN2A, CHEK2, EPCAM, GREM1, MITF, MLH 1, MSH2, MSH6, MUTYH, NBN, PALB2, PMS2, POLE, POLD1, PTEN, RAD51C, RAD51D, SMAD4, STK11, TP53 | https://www.color.com/individuals- genomics | ||
| Hereditary Prostate Cancer Panel | 2 sem | Establece el riesgo de cáncer de próstata a temprana edad, el CaP metastásico/agresivo con riesgo familiar | GeneDX | ATM, BRCA1, BRCA2, BRIP1, CHEK2, EPCAM, HOXB13, MLH1, MSH2, MSH6, NBN, PALB2, PMS2, RAD51C, RAD51D, TP53 | https://providers.genedx.com/tests/detail/hereditary- prostate- cancer- panel- 875 | ||
| myRisk | 2 sem | Establece el riesgo de desarrollar 8 cánceres hereditarios: próstata, mama, ovario, gástrico, colorrectal, páncreas, melanoma y endometrio | Myriad Genetics | APC, ATM, AXIN2, BARD1, BMPR1A, BRCA1, BRCA2, BRIP1, CDH1, CDK4, CDKN2A, CHEK2, EPCAM, GREM1, HOXB13 GALNT12, MLH1, MSH2, MSH3 | https://myriad.com/genetic-tests/myrisk- hereditary- cancer- risk- test/ | ||
| MSH6, MUTYH, NBN, NTHL1, PALB2, PMS2, POLE, POLD1, PTEN, RAD51C, RAD51D, RNF43, RPS20, SMAD4, STK11, TP53 | |||||||
| Prostate Cancer Comprehensive Panel | 2 a 3 sem | Identificar únicamente las variantes hereditarias de la línea germinal que generan riesgo de CaP | Fulgent | ATM, BRCA1, BRCA2, CHEK2, EPCAM, HOXB13, MLH1, MSH2, MSH6, NBN, PMS2, TP53 | https://www.preventiongenetics.com/testInfo?val= Prostate- Cancer- Panel | ||
| Prostate Cancer Panel | 2 a 3 sem | Detectar individuos con una variante patogénica de la línea germinal y no está validada para detectar mosaicismo por debajo del nivel del 20% | Invitae | ATM, BRCA1, BRCA2, CHEK2, EPCAM, HOXB13, MLH1, MSH2, MS6, NBN, PMS2, TP53 | https://www.fulgentgenetics.com/comprehensivecancer- prostate | ||
| Prostate Cancer Panel | 3 a 3 sem | Identificar únicamente las variantes hereditarias de la línea germinal que generan riesgo de CaP | Prevention Genetics | ATM, BRCA1, BRCA2, BRIP1, CHEK2, EPCAM, HOXB13, MLH1, MSH2, MSH6, NBN, PALB2, PMS2, RAD51C, RAD51D, TP53 | https://www.preventiongenetics.com/testInfo?val= Prostate- Cancer- Panel | ||
| Prostate Next | 4 a 3 sem | Ofrece más precisión para identificar y controlar el cáncer de próstata hereditario | Ambry Genetics | ATM, BRCA1, BRCA2, CHEK2, EPCAM, HOXB13, MLH1, MSH2, MSH6, NBN, PALB2, PMS2, RAD51D, TP53 | https://www.ambrygen.com/providers/genetic- testing/5/oncology/prostatenext | ||
| Biomarcadores en tejido | FoundationOneCDx | 8 días | Permite definir terapias apropiadas con evidencia de resistencia, en función del perfil genómico individual del cáncer | Illumina HiSeq 4000 | BRCA1, BRCA2, ATM, BARD1, BRIP1, CDK12, CHEK1, CHEK2, FANCL, PALB2, RAD51B, RAD51C, RAD51D y RAD54L | https://www.foundationmedicine.com/test/foundationone- cdx | |
| Metamark Genetics | 4 sem | Permite generar el pronóstico basándose en proteínas para la progresión del CaP, utiliza inmunofluorescencia múltiple y cuantifica los valores de 8 biomarcadores proteicos combinándolos con el score Gleason (3+) para definir la agresividad | ProMark | CUL2, DERL1, FUS, PDSS2, YBOX1, HSPA9, SMAD4, pS6 | https://promarktest.com/ProMarkCTR/ AssayOverview | ||
| Myriad genetics | 2 a 4 sem | Proporciona información genómica personalizada sobre cómo se comporta el cáncer considera la | Prolaris prostate | ASPM, CDC2, CDCA8, CDKN3, DTL, FOXM1, KIAA0101, NUSAP1, PRC1, TK1 | https://www.dlongwood.com/productos/prolaris/ | ||
| información de puntaje del score Gleason, el valor del PSA y la combina una puntuación molecular obtenida a partir del análisis de la expresión de 16 genes (10 genes relevantes para la actividad tumoral en el ciclo celular y 6 genes de control) | |||||||
| Oncotype Dx Prostate | 6 sem | Analiza 12 genes relacionados con CaP y 5 genes constitutivos, en tejido obtenido por biopsia prostática por punción, y entrega un GPS que va de 0 a 100 para determinar el riesgo | Genomic Health, Redwood City, CA | FAM13C, KLK2, AZGP1, SRD5A2, BGN, COL1A1, SFRP4, ARF, ATP5E, CLTC, GPS1, PGK1, FLNC, GSN, TPM2, GSTM2, TPX2. | https://southgenetics.com/oncotype-dx-gps/ | ||
| ProstaVysion | 2 a 4 sem | Examina dos mecanismos de carcinogénesis de próstata: la fusión/translocación del gen ERG y la pérdida del gen supresor de tumores PTEN, para determinar tratamiento | Bostwick Laboratories, Glen Allen, VA | ERG, PTEN. | https://www.bu.edu/shipley/prostate-cancer-testing/available-tests/genetic-tests/prostavysion/ | ||
| UW OncoPlex Cancer Gene Panel | 4 a 6 sem | Detectar la mayoría de las clases de mutaciones, incluidas variantes de un solo nucleótido, pequeñas inserciones y eliminaciones (indeles), amplificaciones de genes y fusiones de genes seleccionados. Permite orientar el tratamiento y la estadificación del cáncer de próstata | NGS | ABL1, AKT1, APC, ARID1A, ARID1B, ATM, ATR, AURKA, BAP1, BCL2, BRCA1, CCND1, DDR2, EGFR, ERBB4, FLT3, FOXP3, GATA1, GNA11, GNAQ, HER- 2, IDH1, IDH2, JAK1, KRAS, MSI, NRAS, PIK3CA, TMB, TP53, mTOR. | https://testguide.labmed.uw.edu/view/OPX?tabs=no | ||
|
CaP: cáncer de próstata; PSA: antígeno prostático específico; GPS: genomic prostate score; MSI: inestabilidad de microsatélites; TMB: carga total de mutaciones; CA: California; VA: Virginia; Inc: Sociedad Anónima. |
|||||||
Los paneles de la búsqueda comparten varios biomarcadores específicos conocidos de CaP como el PCA3, TMPRSS2. En la figura 3 se evidencia la distribución por frecuencia de los principales biomarcadores asociados a la reparación del ADN vinculados con la proliferación, supervivencia, migración y metástasis (BRIP1, CDK1, CCND1, PTEN, PALB2, CHEK2, SMAD4, TP53, NBN, KLK) y los biomarcadores asociados a la detección de variantes patogénicas de líneas germinales (BRCA1/2, ATM, MLH1, MSH2, MSH6, PMS2, EPCAM, HOXB13, CDKN2A).
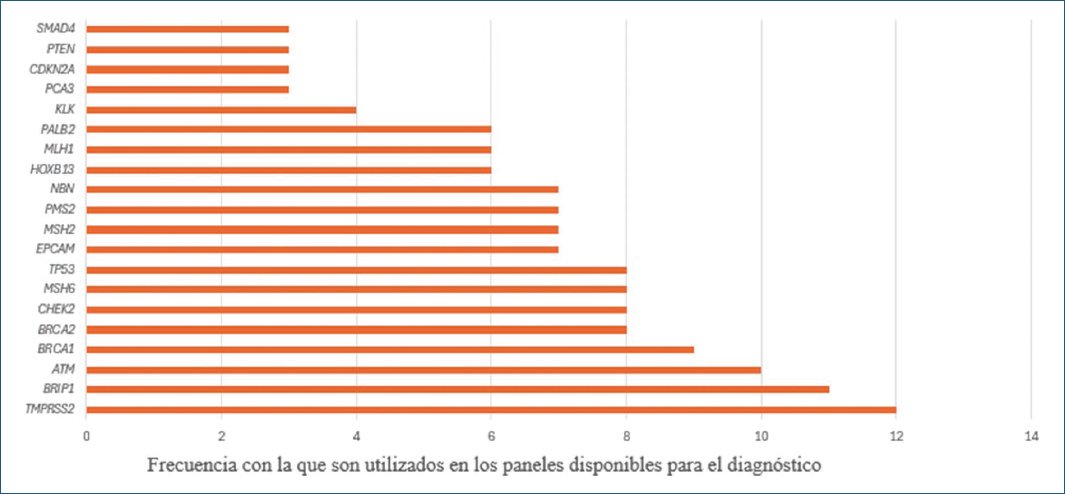
Figura 3. Genes identificados en los paneles genéticos, distribuidos de acuerdo con la frecuencia en la que son utilizados en los paneles disponibles para el diagnóstico.
Considerando la utilidad clínica de los paneles genéticos, se realizó una búsqueda y recopilación de 21 artículos (Tabla 2)28–48, que evidenciaron la implementación de distintos paneles genéticos en distintas poblaciones, permitiendo establecer la gravedad e implementar una terapia dirigida en el CaP. Esta búsqueda abarcó estudios observacionales, de casos y control, reporte de un caso y estudios de cohorte.
Tabla 2. Estudios que emplean plataformas masivas para la asociación diagnóstica, pronóstica y tratamiento del CaP
| Año | Título | Tipo de estudio | Objetivo | Edad y/o etnia o nacionalidad | Muestra/casa comercial/instrumento | Alteración genética | Aplicabilidad | Referencia |
|---|---|---|---|---|---|---|---|---|
| 2014 | Frequent germline deleterious mutations in DNA repair genes in familial prostate cancer cases are associated with advanced disease | Cohorte retrospectiva | Evaluar las mutaciones nocivas en los genes supresores de tumores en CaP familiar y estimar el riesgo. | Edad media: 58,5 años. Etnia: 131 europea-blanca, 2 africanos negra, 3 caribeña negra 1 asquenazí | 191 muestras de sangre/Illumina/Ilumina Cbot y Hiseq 2000 | ATM, BRCA1, BRCA2, BRIP1, CHEK2, MUTYH, PALB2, PMS2. | Estadificación de riesgo y heredabilidad | 28 |
| 2015 | Comprehensive serial molecular profiling of an “N of 1” exceptional non-responder with metastatic prostate cancer progressing to small cell carcinoma on treatment | Reporte de caso | Identificar genes causantes de un caso de CaP de inicio temprano que progresó rápidamente a NePC | Edad: 47 años. Nacionalidad: estadounidense | 1 muestra de tejido prostático y de tejido hepático/Thermo Fisher Scientific/PCR (Ampliseq) utilizando ADN de 40 ng y el Panel Integral de Cáncer (CCP) Ion Torrerent | TP53, SMAD4, KMT2D; MTRR JAK3, NOTCH4. | Estadificación supervivencia | 29 |
| 2017 | Molecular testing in patients with castration-resistant prostate cancer and its impact on clinical decision making | Cohorte | Abordaje terapéutico del CaP metastásico resistente a la castración (CRPC) utilizando pruebas mutacionales y de IHQ de PTEN | Edad media: 70 años. Edad: 49 a 87 años. Nacionalidad: estadounidense | 46 muestras de tejidos/Laboratorios de diagnóstico Knight/Genetrails solid tumor panel | TP53, PTEN, TSC2, FGFR3, NOTCH1, RB1.CDK | Tratamiento | 30 |
| 2018 | Rare germline genetic variants and risk of aggressive prostate cancer | Cohorte | Identificar variantes hereditarias raras que distinga entre estos dos fenotipos extremos, mediante la secuenciación de exomas | Rango de edad: 54 a 71 años. Nacionalidad: estadounidense | 280 muestras de ADN de la línea germinal de CaP/Illumina/HiSeq 2500 instrument | ATM, BRCA2, CHEK2, NBN, PALB2, PMS2, PRSS1, RAD51D; XRCC2, PMS2, LUM | Diagnóstico | 31 |
| 2019 | Rare germline variants in DNA repair genes and the angiogenesis pathway predispose prostate cancer patients to develop metastatic disease | Cohorte | Identificar variantes hereditarias raras que distinga entre estos dos fenotipos extremos, mediante la secuenciación de exomas | Rango de edad: 54 a 71 años. Nacionalidad: estadounidense | 280 muestras de ADN de la línea germinal de CaP/Illumina/HiSeq 2500 instrument | ATM, BRCA2, CHEK2, NBN, PALB2, PMS2, PRSS1, RAD51D; XRCC2, PMS2, LUM | Diagnóstico | 32 |
| 2019 | Genomic analysis of Korean patients with advanced prostate cancer by use of a comprehensive next-generation sequencing panel and low-coverage, whole-genome sequencing | Retrospectivo/banco de muestras | Analizar los perfiles de mutación en pacientes coreanos con CaP metastásico mediante un análisis de LC-WGS | Rango de edad 53 a 88 años. Etnia: coreana | 14 muestras de tejido y 2 muestras de sangre periférica/ThermoFisher Scientific/la secuenciación del genoma completo de baja cobertura (LC-WGS)/El Panel Integral de Oncomine/NextSeq 500 | TP53, SPOP, PTEN, APC, AR, CTNNB1., AKT1, KRAS, NRAS, STK11, RB1. | Tratamiento | 33 |
| 2020 | Genomic profiles of de novo high- and low-volume metastatic prostate cancer: results from a 2-stage feasibility and prevalence study in the STAMPEDE trial | Cohorte retrospectivo y prospectivo | Establecer las alteraciones genómicas iniciales en un estudio en 2 etapas, mediante tNGS en el CaP | Edad media 68 años. Etnia: anglosajones/americanos | 1ª cohorte: 185 muestra de tejido prostático. 2.ª cohorte: 93 muestras de tejido prostático y 89 muestras de saliva/Almac Diagnostics (Craigavon, Reino Unido)/panel TST-170, panel de 30 genes clínicamente acreditado (Color Genomics) | TP53, PTEN, APC, CTNNB1, SPOP, RB1, KMT2C/MLL3, CHEK, SPOP, CDK12, ETS, WNT | Estadificación supervivencia | 34 |
| 2020 | Clinical and genomic insights into circulating tumor DNA-based alterations across the spectrum of metastatic hormone-sensitive and castrate-resistant prostate câncer | Cohorte prospectiva | Identificar mediante ctDNA las variaciones genéticas CaP metastásico progresivo | Edad media 66 años; rango 45-90. Nacionalidad: estadounidense y australiana | 250 muestras de sangre periférica/Agilent Technologies/panel PredicineLDT/Bioanalyzer 2100 | EGFR, MYC, CDK6, APC, KIT, APC, RBI1, CDK12, ARID1A, NF1, PTEN y genes de reparación del ADN (ATM, BRCA1, BRCA2 y CHEK2) Genes en las 2 poblaciones TP53, AR, BRCA2 y BRAF. | Estadificación supervivencia | 35 |
| 2020 | High prevalence of DNA damage repair gene defects and TP53 alterations in men with treatment-naïve metastatic prostate cancer -Results from a prospective pilot study using a 37 gene panel | Cohorte | Identificar genes de puntos de control y reparación de daños en el ADN de 37 genes en condiciones de rutina mediante NGS | Edad media 56 años; rango 40-80 años. Nacionalidad: alemana | 64 muestras de tejido/Thermo Fisher Scientific/Oncomine BRCA y un panel patentado (HRDv1) que se desarrolló para el presente estudio | TP53, CHEK2, FANCL, FANCM, XRCC2, RECQL4, ERCC2, SLX4, ATM, FANCA, FANCG, BRCA2, ATM, ERCC4, MSH2, MSH6, RECQL4 y SLX4. | Diagnóstico | 36 |
| 2020 | Targeted next-generation sequencing for locally advanced prostate cancer in the Korean population | Casos | Evaluar la viabilidad del análisis de panel pancáncer para el CaP localmente avanzado en la población coreana | Edad media 69 años; rango 55 a 83 años. Nacionalidad: coreana | 20 muestras de tejido/Illumina/Bioanalyzer 2100/Illumina Hiseq 2500 | SPOP, KMT2D, ATM, BRAF, FANCA, FANCD2, FANCG, MAP3K1, TSHR, ERG. TP53 y PTEN | Diagnóstico y tratamiento | 37 |
| 2021 | Cell-free DNA variant sequencing using plasma and AR-V7 Testing of circulating tumor cells in prostate cancer patients | Cohorte | Asociación en el pronóstico de CaP mediante de cfDNA y CTC | Edad media 67 años; rango 48-89 años. Nacionalidad: alemana | 39 muestras de sangre/Illumina/NextSeq 500 | MUC16 (56 variantes); AR (32 variantes); TP53 (15 variantes) | Estadificación supervivencia | 38 |
| 2021 | TP53 alterations of hormone-naïve prostate cancer in the Chinese population | Casos | Establecer el papel de TP53 en el CaP primario sin tratamiento hormonal en poblaciones china y occidental | Edad media 68 años; rango 51 a 87 años. Nacionalidad: china | 101 muestras de tejidos/Illumina | MAP2K4, NLRP1, RNF43, SYNE1, FANCG, ARID1A, NCOR2, BCOR2 | Estadificación de riesgo y tratamiento | 39 |
| 2021 | Genomic mutation profiling using liquid biopsy in Korean patients with prostate cancer: circulating tumor DNA mutation predicts the development of castration resistance | Cohorte | Definir los perfiles de mutación somática y de la línea germinal en pacientes coreanos con CaP mediante ctDNA | Rango de edad: 65 a 77 años. Nacionalidad: coreana | 56 muestras de plasma y 18 muestras de tejidos/Thermo Fisher Scientific/Oncomine/Recover All (143 genes) | TP53, PIK3CA, TMPRSS2-ERG, MYC, FGFR3, MET, IDH1, SMAD4, SF3B1, RAD50 y BRCA1 | Estadificación supervivencia | 40 |
| 2022 | TP53 alterations of hormone-naïve prostate cancer in the Chinese population | Cohorte | Establecer la prevalencia de mutaciones de la línea germinal para CaP en población turca | Edad media: 64,7. Nacionalidad: turca | 21 muestras de sangre/Illumina/MiSeq Reagent Nano Kit v2 | BRCA2, APC, AR, BRIP1 CHEK2, EHBP1, FANCA, FGFR4, ITGA6, MSH6, PLXNB1, POLE, POLD1 | Estadificación riesgo y progresión | 41 |
| 2022 | Comprehensive genomic profiling of treatment resistant metastatic castrate sensitive prostate cancer reveals high | Cohorte | Explorar la viabilidad y utilidad potencial de ADT en mCSPC | Edad media 63 años; rango 47 a 83 años. Etnia: caucásica, afroamericana, asiática | 24 muestras de tejido/Illumina; Thermo Fisher Scientific/ Paneles: UHN Hi5 y OCAv3/NextSeq (UHN Hi5); 2. Ion Torrent S5 XL | BRCA2; ATM; CDK12; ATR; SPOP; FOXP1; TP53, ARAT | Estadificación supervivencia/tratamiento | 42 |
| frequency of potential therapeutic targets | (Oncomine Comprehensive Assay v3, OCAv3) | |||||||
| 2022 | PIN-like ductal carcinoma of the prostate has frequent activating RAS/RAF mutations | Casos | Perfilar molecularmente los casos de carcinoma ductal tipo PIN en prostatectomía radical | Edad media 60 años; rango 45 a 72 años. Nacionalidad: estadounidense | 5 muestras de tejidos/Illumina/HiSeq 2500 instrument | BRAF, ARID1A, CREBBP, HRAS, MAP2K4, NCOR2, MAP3K6, EP300 | Diagnóstico | 43 |
| 2023 | Early plasma circulating tumor DNA as a potential biomarker of disease recurrence in non-metastatic prostate cancer | Estudio observacional | Evaluar la utilidad clínica del cfDNA para predecir la recurrencia del CaP | Edad media 66 años; rango 61,5 a 70,5 años. Nacionalidad: china | 139 muestras de sangre periférica y 31 muestras de tejido protático/Illumina/Nextseq500 or Novoseq 6000 | NCOR2, BRCA2, ATR y CDK12, TP53 y PTEN | Estadificación de recurrencias y supervivencia | 44 |
| 2023 | Investigation of clinically significant molecular aberrations in patients with prostate cancer: implications for personalized treatment, prognosis and genetic testing | Cohorte | Evaluar la prevalencia de variantes patogénicas de la línea germinal somáticas clínicamente relevantes en pacientes con CaP metastásico, localmente avanzado o de alto grado y evaluar su papel pronóstico y predictivo en esos pacientes | Edad media 69,6 años; rango 46,8 a 95 años. Nacionalidad: estadounidense | 196 muestras de tejido y 5 muestras de sangre periférica/Medicover genetics/Ampliseq IAD207308_231./Secuenciación de Sanger (ABI 3130×l) | ATM, BRCA2, BRCA1, TMPRSS2-ERG, CTNNB1, MSH2, PIK3CA, PTEN y TP53. l Línea germinal: RAD51C y ATM | Diagnóstico, estadificación riesgo y supervivencia | 45 |
| 2023 | Multi-gene next-generation sequencing panel for analysis of BRCA1/BRCA2 and homologous recombination repair genes alterations metastatic | Cohorte | Establecer la eficacia del panel genético en la caracterización molecular del CaP | Edad media 63,8 años; rango 40 a 80 años. Nacionalidad: italiana | 49 muestras de tejido/Thermo Fisher Scientific/Panel específico de tumores Oncomine personalizado | BRCA2, ATM, BRCA1, ARID1A, BAP1, BARD1, BRIP1, CHEK2, CDK12, FANCA, FANCL, MLH1, PALB2, PIK3CA, PMS2, PPP2R2A | Diagnóstico y tratamiento | 46 |
| castration-resistant prostate cancer | ||||||||
| 2023 | DKK3’s protective role in prostate cancer is partly due to the modulation of immune-related pathways | Cohorte retrospectiva | Identificar mecanismos por medio de los cuales Dickkopf-3 (DKK3) produce su posible papel protector en el CaP utilizando NGS | Edad media 67 años; rango 56 a 94 años. Nacionalidad: 9 egipcios, 3 emiratíes, 1 palestino, 1 sudanes | 14 muestras de tejido/1.Thermo Fisher Scientific/2. Zymo Research/Secuenciador Ion S5 XL Semiconductor utilizando el chip Ion 540 | DKK3, IRAK1, RIOK1 | Estadificación supervivencia | 47 |
| 2023 | Implementation of a prostate cancer-specific targeted sequencing panel for credentialing of patient-derived cell lines and genomic characterization of patient samples | Cohorte | Validar la utilidad de un panel específico para identificar características genómicas del paciente y las líneas celulares derivadas en el CaP | Edad media 63 años; rango de edad 52 a 72 años. Nacionalidad: norteamericano | 30 muestras de tumor fresco congelado; 2 muestras de ADN de CaP, 4 muestras de CTC de mPCa; 2 muestras cfDNA y 8 líneas celulares de próstata | KRAS Q61R, TP53 R273G, CTNNB1, K335I, SPOP, FOXA1, Y177C; KDM6A, EGFR, CDKN1B NCOR1, ATM (APC SCN11A (PIK3CA) y CDKN1B (TMPRSS2-ERG, CHD1, PTEN, RB1 y BRCA2. MYC | Diagnóstico | 48 |
|
ADT: terapia de privación de andrógenos; AR-V7: variante de empalme del receptor de andrógenos-7 la castración; CaP: cáncer de próstata; CGP: perfil genómico integral; CNA: número de copias; CTC: células tumorales circulantes; cfDNA: ; ctDNA: ; DKK3: Dickkopf-3; IHQ: inmunohistoquímica; LC-WGS: la secuenciación del genoma completo de baja cobertura; LoF: mutaciones por pérdida de función; mCRPC: cáncer de próstata metastásico resistente a la castración; mCRPC: cáncer de próstata resistente a hormonas; mCSPC: cáncer de próstata metastásico sensible a la castración; mHSPC: cáncer de próstata sensible a hormonas; mPCa: cáncer de próstata metastásico; NePC: carcinoma de células pequeñas/cáncer de próstata neuroendocrino; NGS: secuenciación de nueva generación; nmPCa: cáncer de próstata no metastásico; PIN: mneoplasia intraepitelial prostática; SG: supervivencia general; SNV: variación en la secuencia de ADN de 1 nucleótido; NGS: secuenciación de nueva generación; VUS: variantes de significado incierto. |
||||||||
En los artículos analizados se encontró una alta prevalencia de mutaciones en los genes que reparan el ADN (ATM, BRCA2, BRIP1, CHEK2, PMS2, RAD51C, TP53), de la vía PI3K y de la vía de señalización RAS/RAF/MAPK, especialmente el gen MUTYH, que se asoció a gravedad, mientras que las mutaciones de la línea germinal en mayor frecuencia son ATM, BRCA2, BRIP1, CHEK2, PMS2, RAD51C y TP53, considerando que las poblaciones que han participado en estos estudios son principalmente américa-anglosajones y asiáticos, evidenciándose la poca o nula existencia de estudios que involucren población latina.
Es importante destacar que en poblaciones asiáticas se ha evidenciado mayor frecuencia de alteraciones en: TP53, PIK3CA, TMPRSS2-ERG SPOP, BRAF y AR, esto le confiere un perfil genético de con mayor agresividad, mientras que en poblaciones negras predominan mutaciones en BRCA1, BARD1, BRCA2 y PMS2, lo que le confiere una mayor heredabilidad, a diferencia de las poblaciones occidentales, donde las mutaciones se presentan con mayor frecuencia en los genes TP53, AR, BRCA2 y BRAF, asociándose a una progresión más rápida de la enfermedad49.
La figura 4 indica la distribución de los paneles con base en su aplicabilidad y el tipo de variante o mutación genética somática o de la línea germinal para su abordaje en el diagnóstico y tratamiento del CaP, encontrando que las variantes asociadas a los genes APC, AR, CTNNB1, MTOR, DHRS2, NBN, PTEN, RB1, RAD50, PARK2, SPOP, SMAD4 y TMPRSS2-ERG permiten diagnóstico, estadificación y tratamiento, y se correlacionan en mayor medida con mutaciones somáticas, mientras que variantes asociadas a los genes ATM, BRCA2, BRIP1, CHEK2, PMS2, RAD51C y TP53 se asocian a susceptibilidad de herencia, distinguiéndose mutaciones de la línea germinal.
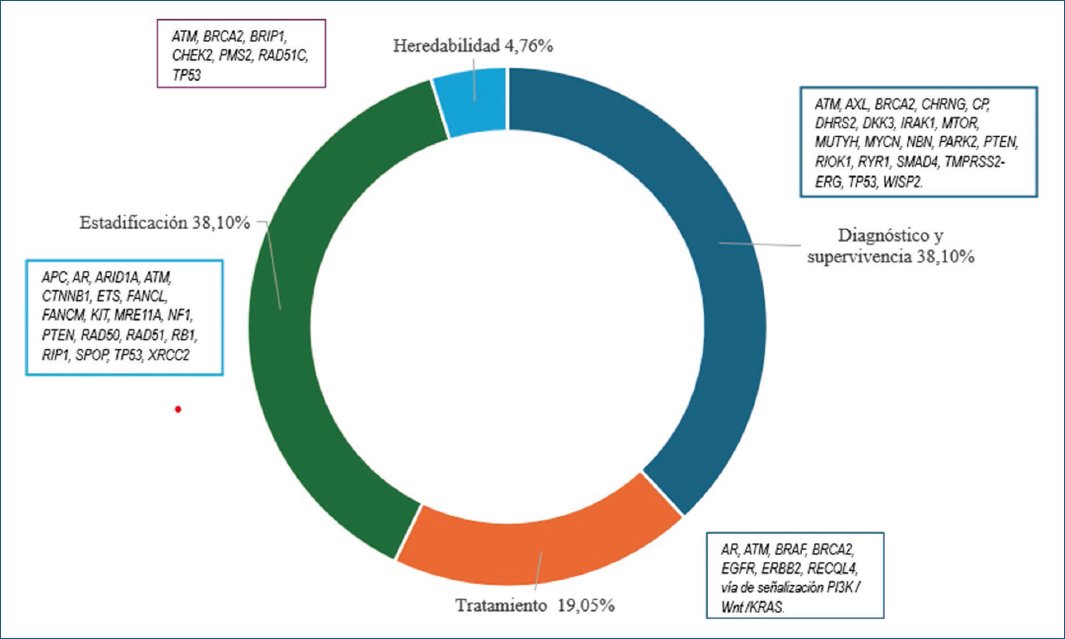
Figura 4. Porcentaje de recurrencia de genes en los que se han identificado variantes genéticas patogénicas con aplicabilidad en el cáncer de próstata. La figura muestra los genes de acuerdo con heredabilidad, diagnóstico y supervivencia, tratamiento y estadificación. El porcentaje está calculado con base en los artículos usados para el análisis que se detalla en la tabla 1.
La proporción de casos de CaP atribuible al CaP hereditario es de alrededor de un 5-15%, de los cuales un 5% aproximadamente de un CaP localizado de alto riesgo tienen mutaciones germinales en genes de reparación del ADN como: BRCA2, CHEK2, ATM, BRIP1, HOXB13, RAD51, BRCA1 y PALB250.
Hallmarks en el cáncer de próstata
En el año 2000, Douglas Hanahan y Robert Weinberg publicaron el artículo The hallmarks of cancer. En él se conceptualizan seis reglas básicas para la transformación en múltiples pasos de las células normales en células tumorales, las cuales comprenden: mantener la señalización proliferativa, evadir los supresores del crecimiento, resistir la muerte celular, permitir la inmortalidad replicativa, inducir o acceder a la vasculatura, activar la invasión y la metástasis, desregular el metabolismo celular y evitar la destrucción inmunitaria51.
El estudio molecular del cáncer ha permitido identificar tres factores principales que pueden explicar la consecución del estado de autosuficiencia en la señalización del crecimiento o el mantenimiento de la señalización proliferativa en el CaP: el funcionamiento aberrante del receptor de andrógenos, la modulación de la actividad del receptor del factor de crecimiento y la modulación de un circuito de señalización intracelular alternativo asociado con el crecimiento, la supervivencia y la proliferación celular52. Es por ello que, con base en la mayor frecuencia encontrada en los estudios analizados, se ha determinado los 10 genes con mutaciones somáticas y 10 genes de la línea germinal, profundizado las características y sus funciones considerando las bases de datos COSMIC (catálogo de mutaciones somáticas)53, The Gene CC (define función y ecanismos genéticos)54, COSMIC, Hallmarks of Cancer (rol del gen en el desarrollo del cáncer)53 y OMIM (utilidad de los genes en una enfermedad)55, que se visualizan en la tabla 3.
Tabla 3. Genes asociados a mutaciones somáticas y germinales en el cáncer de próstata
| Gen | Nombre completo53 | Ubicación55 | Hallmarks53 | Clasificación Gen CC54 | ||||
|---|---|---|---|---|---|---|---|---|
| Función | P | S | Relación gen-enfermedad/MIM fenotipo | Herencia | ||||
| Germinales | ||||||||
| ATM | Gen mutado de ataxia telangiectasia | 11q22.3 | Fosforila la histona H2AX en respuesta a roturas de doble cadena del ADN, reparación de roturas de doble hebra del ADN, recluta y coopera con otras proteínas censoras | 4, 5, 9 | 6, 8 | Limitada | Autosómica dominante | |
| BRCA1 | Cáncer de mama 1 «breast cancer 1» | 17q21.31 | Reparación de daños en el ADN y proteína nuclear de control del ciclo celular, maquinaria transcripcional | 6, 1 | 7, 8, 9 | n/a | n/a | |
| BRCA2 | Cáncer de mama 2 «breast cancer 2» | 13q13.1 | Proteína reparadora de daños en el ADN | – | 8, 9 | Definitivo (176807) | Autosómica dominante | |
| CHEK2 | Homólogo del punto de control CHK2 «checkpoint kinase 2» | 22q12.1 | Tras el daño del ADN, CHK2 es fosforilada por ATM o ADN-PKcs y se activa en la reparación del ADN, la regulación del ciclo celular, la señalización de p53 y la apoptosis | – | 8, 9 | n/a | ||
| HOXB13 | «Homeobox 13» | 17q21.32 | n/a | n/a | n/a | n/a | n/a | |
| EPCAM | Molécula de adhesión celular epitelial «epithelial cell adhesion molecule» | 2p21 | n/a | n/a | n/a | n/a | Autosómica dominante | |
| MLH1 | Mutaciones en genes reparadores MMR «mutL Homology 1» | 3p22.2 | Participan en el reconocimiento y reparación de desajustes de pares de bases y pequeños indeles que surgen durante la replicación del ADN | 2 | 6, 8, 9 | Relación discutible (120436) | Autosómica dominante | |
| MSH2 | Mutaciones en genes reparadores MMR «mutL Homology 2» | 2p21-p16.3 | Componente de los complejos MutS-alfa y -beta que participan en el reconocimiento posterior a la replicación y en la reparación de desajustes de bases y bucles de inserción/eliminación | 2, 4, 5, 9 | 3, 8, 9 | Moderado (609309) | Autosómica dominante | |
| MSH6 | Mutaciones en genes reparadores MMR «mutL Homology 6» | 2p16.3 | Forma un heterodímero con MSH2 en el complejo MutS-alfa, Participa en el reconocimiento y reparación tras la replicación de desajustes de bases y bucles de inserción/deleción | 1, 2, 6, 9 | 3, 8 | Limitada (600678) | Autosómica dominante | |
| TP53 | Proteína tumoral P53 «Tumor protein p53» | 17p13.1 | Factor de transcripción que coordina la respuesta celular al estrés causado por una variedad de señales que incluyen daño al ADN, señalización aberrante del crecimiento, hipoxia y una amplia gama de fármacos quimioterapéuticos, luz ultravioleta e inhibidores de la proteína cinasa | 2, 4, 9, 10 | 3, 4, 5, 6, 7, 8, 9 | n/a | n/a | |
| PMS2 | Segregación posmeiótica aumentada 2 «Post-Meiotic Segregation Increased 2» | 7p22.1 | Proteína reparadora de desajustes de ADN | 2 | 6, 8, 9 | Limitada (600259) | Autosómica dominante | |
| Genes mutaciones somáticas | ||||||||
| NBN | Síndrome de rotura de Nijmegen «Nijmegen breakage syndrome» | 8q213 | n/a | n/a | n/a | n/a | n/a | |
| RAPGEF4 | Factor de intercambio de nucleótidos de guanina rap 4 «Rap Guanine Nucleotide Exchange Factor 4» | 2q31.1 | n/a | n/a | n/a | Limitado (606058) | Autosómica dominante | |
| RNASEH2B | Ribonuclease H2 de la subunit b del RNASEH2B «Ribonuclease h2, subunit b» | 13q14.3 | n/a | n/a | n/a | limitada (610326) | Autosómica dominante | |
| PTEN | Proteína homologa de la fosfatasa y tensina «Phosphatase and tensin homolog» | 10q23.31 | Cataliza la desfosforilación del fosfatidilinositol-3,4,5-trifosfato, una molécula clave implicada en la señalización del crecimiento celular, específicamente en la posición 3 del anillo de inositol; puede desfosforilar sustratos proteicos en residuos de serina/treonina y tirosina; regula los niveles y la actividad de la proteína p53 por medio de mecanismos dependientes e independientes de la fosfatasa | 2, 10 | 3, 4, 6, 8, 9 | n/a | n/a | |
| CDK4 | Cinasa 4 dependiente de ciclina «Cyclin-dependent kinase 4» | 12q14.1 | Cinasa dependiente de ciclina, regula la progresión mediante la fase G1, esencial para la proliferación de algunas células endocrinas y hematopoyéticas, fosforila: Cdt1, Marcks, p107, p130, pRb y Smad3 | 4 | – | n/a | n/a | |
| CDKN2A | Inhibidor de cinasa dependiente de ciclina 2a «Cyclin-dependent kinase inhibitor 2a» | 9p21.3 | Codifica dos proteínas distintas, p16INK4a y p14ARF, las cuales demuestran actividad supresora de tumores en vías anticancerígenas genéticamente distintas: la vía Rb para p16INK4a y la vía p53 para p14ARF | 2 | 6, 7, 9 | n/a | n/a | |
| MUTYH | «MutY homolog (E. coli)» | 1p34.1 | n/a | n/a | n/a | n/a | n/a | |
| SMAD4 | «SMAD family member 4» | 18q21.2 | Es un mediador central de las vías de señalización canónicas de TGF-beta y BMP | 2, 5, 6, 7 | 6, 7, 8 | n/a | n/a | |
| ULK4 | «Serina/treonina protein Kinase 4» | 3p22.1 | n/a | n/a | n/a | Limitado (617010) | Autosómica dominante | |
| XPO7 | «Exportin 7» | 8p21.3 | n/a | n/a | n/a | Limitado (606140) | Autosómica dominante | |
|
ADN-PKc: la subunidad catalítica de la proteína cinasa dependiente de ADN; BMP: proteína morfogénica ósea; MMR: sistema de reparación de errores de emparejamiento; p: brazo corto del cromosoma; P: promotores; q: brazo largo del cromosoma; S: supresores; TGF-beta: factor de crecimiento transformante beta. Hallmarks: 1, señalización proliferativa; 2, supresión del crecimiento; 3, escapar de la respuesta inmunitaria al cáncer; 4, inmortalidad replicativa celular; 5, tumor que promueve la inflamación; 6, invasión y metástasis; 7, angiogénesis; 8, inestabilidad del genoma y mutaciones; 9, escapar de la muerte celular programada; 10, cambio de energía celular. |
||||||||
Independientemente del tipo de mutación que se presente en el CaP se evidencia un patrón de herencia autosómica dominante, las mutaciones que se originan en genes de la línea germinal se asocian principalmente a cambios en la reparación del ADN, siendo las características promotoras más prevalentes la supresión del crecimiento y escapar de la muerte celular programada; mientras que las características supresoras son la inestabilidad del genoma y mutaciones, así como escapar de la muerte celular programada; a diferencia de lo que sucede con las mutaciones somáticas, que se presentan en genes supresores y codificantes en las vías de señalización, donde las característica promotora establece mayor prevalencia en el cambio de energía celular y la supresión del crecimiento, mientras que las supresoras se enfocan en la invasión y metástasis en conjunto con la inestabilidad del genoma y mutaciones.
Con respecto a la relación entre el gen y la presencia de enfermedad, se ha corroborado únicamente con el gen BRCA2, y de manera moderada con el gen MSH2, mientras que los genes ATM, MSH6 y PMS2 tienen una relación limitada con el desarrollo de la enfermedad de acuerdo con los datos obtenidos en la base de datos The Gene CC.
Nuevas perspectivas de tratamiento para el cáncer de próstata
La identificación de biomarcadores del cáncer con orientación de mutaciones genéticas específicas ha permitido mejorar las terapias de tratamiento en el cáncer, de manera que se brindan mayores oportunidades en casos avanzados de CaP. Se ha demostrado que la intensificación de la terapia de privación de andrógenos con agentes inhibidores de la vía de los andrógenos (abiraterona, apalutamida y enzalutamida) o quimioterapia (docetaxel) en pacientes con CaP metastásico sensible a la castración (mCSPC) retrasa la progresión de la enfermedad y prolonga la supervivencia del paciente56.
Adicionalmente, se están evaluando biomarcadores aplicados a tratamientos combinados, como la radioterapia junto a nuevas moléculas dirigidas, que permiten intensificar el tratamiento en subgrupos de pacientes con mayor riesgo de progresión, identificándose que las variantes patogénicas de P53 y ATM y la pérdida de PTEN están asociadas con la radiosensibilidad del CaP57.
Los tratamientos enfocados en terapia genética para el CaP permiten un manejo personalizado, enfocándose en el diagnóstico temprano, y mejoran las tasas de supervivencia y la calidad de vida de los pacientes.
Conclusión
El uso de OMIC en el diagnóstico y tratamiento del CaP ha revolucionado el campo de la oncología al permitir una mejor comprensión de la heterogeneidad molecular de la enfermedad. Las tecnologías de secuenciación, en especial la NGS, han facilitado la identificación de alteraciones en genes de reparación de ADN y en vías de señalización claves, proporcionando herramientas para tratamientos personalizados que mejoran los resultados clínicos y la supervivencia de los pacientes.
El desarrollo de paneles genéticos ha mostrado beneficios en la predicción del riesgo hereditario y la selección de terapias dirigidas, sin embargo se requiere mayor investigación en poblaciones diversas especialmente a nivel de Latinoamérica, para optimizar la aplicabilidad de estas herramientas.
Agradecimientos
Los autores agradecen a la Universidad Técnica Particular de Loja, por brindar al asesoramiento metodológico necesario para la elaboración del presente artículo.
Financiamiento
Los autores declaran que este trabajo se realizó con recursos propios.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales de pacientes ni requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
